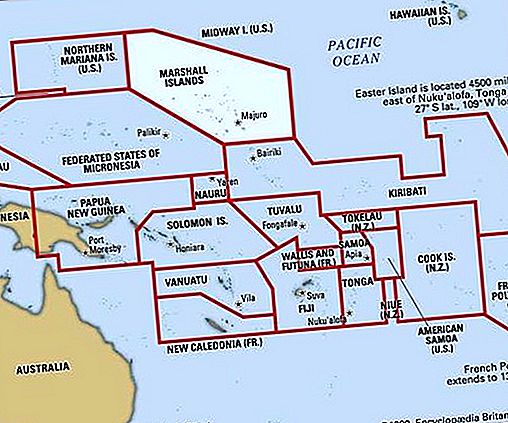
Cryopreservation, konservering af celler og væv ved frysning.

Sir Ian Wilmut: Uddannelse og kryokonserveringsforskning
Wilmut blev opvokset i Coventry, en by i det historiske engelske amt Warwickshire, og han gik på Agricultural College på universitetet
Kryopreservation er baseret på visse små molekylers evne til at komme ind i celler og forhindre dehydrering og dannelse af intracellulære iskrystaller, hvilket kan forårsage celledød og ødelæggelse af celleorganeller under fryseprocessen. To almindelige kryobeskyttelsesmidler er dimethylsulfoxid (DMSO) og glycerol. Glycerol bruges primært til kryobeskyttelse af røde blodlegemer, og DMSO bruges til beskyttelse af de fleste andre celler og væv. Et sukker kaldet trehalose, der forekommer i organismer, der er i stand til at overleve ekstrem dehydrering, bruges til frysetørringsmetoder til kryokonservering. Trehalose stabiliserer cellemembraner, og det er især nyttigt til konservering af sædceller, stamceller og blodlegemer.
De fleste systemer med cellulær kryokonservering bruger en fryser med kontrolleret hastighed. Dette frysesystem leverer flydende nitrogen i et lukket kammer, hvori cellesuspensionen er anbragt. Omhyggelig overvågning af frysningshastigheden hjælper med at forhindre hurtig cellulær dehydrering og dannelse af iskrystaller. Generelt tages cellerne fra stuetemperatur til ca. -90 ° C (-130 ° F) i en fryser med kontrolleret hastighed. Den frosne cellesuspension overføres derefter til en fryser med flydende nitrogen fastholdt ved ekstremt kolde temperaturer med nitrogen i enten dampen eller væskefasen. Kryopreservation baseret på frysetørring kræver ikke anvendelse af flydende nitrogenfrysere.
En vigtig anvendelse af kryopræservering er frysning og opbevaring af hæmatopoietiske stamceller, som findes i knoglemarven og perifert blod. Ved autolog knoglemarvsredning opsamles hæmatopoietiske stamceller fra en patients knoglemarv inden behandling med højdosis kemoterapi. Efter behandling optøes patientens kryokonserverede celler og infunderes tilbage i kroppen. Denne procedure er nødvendig, da kemoterapi med høj dosis er ekstremt giftig for knoglemarven. Evnen til kryopræservering af hæmatopoietiske stamceller har i høj grad forbedret resultatet for behandlingen af visse lymfomer og maligniteter i fast tumor. For patienter med leukæmi er deres blodlegemer kræftfremkaldende og kan ikke bruges til autolog knoglemarvsredning. Som et resultat er disse patienter afhængige af kryokonserveret blod opsamlet fra navlestrengsnorene hos nyfødte spædbørn eller på kryokonserverede hæmatopoietiske stamceller opnået fra donorer. Siden slutningen af 1990'erne er det blevet erkendt, at hæmatopoietiske stamceller og mesenkymale stamceller (afledt af embryonalt bindevæv) er i stand til at differentiere i skelet- og hjertemuskelfæv, nervevæv og knogler. I dag er der intens interesse for vækst af disse celler i vævskultursystemer såvel som i kryokonservering af disse celler til fremtidig behandling af en lang række forstyrrelser, herunder forstyrrelser i nervesystemet og muskelsystemerne og lever og hjertesygdomme.
Cryopreservation bruges også til at fryse og opbevare menneskelige embryoner og sædceller. Det er især værdifuldt til frysning af ekstra embryoner, der genereres ved in vitro-befrugtning (IVF). Et par kan vælge at bruge cyropreserverede embryoner til senere graviditeter eller i tilfælde af, at IVF mislykkes med friske embryoner. I processen med frosset embryooverførsel optøes embryonerne og implanteres i kvindens livmoder. Frosset embryooverførsel er forbundet med en lille, men signifikant stigning i risikoen for kræft i børn blandt børn født fra sådanne embryoner.
Dyp hypotermi, en form for mild kryokonservering anvendt hos humane patienter, har betydelige anvendelser. En almindelig anvendelse af induktion af dyb hypotermi er til komplekse kardiovaskulære kirurgiske procedurer. Efter at patienten er blevet anbragt på en komplet kardiopulmonal bypass ved hjælp af en hjerte-lungemaskine, passerer blodet gennem et kølekammer. Kontrolleret afkøling af patienten kan nå ekstremt lave temperaturer på ca. 10-14 ° C (50–57 ° F). Denne mængde afkøling stopper effektivt al cerebral aktivitet og giver beskyttelse for alle vitale organer. Når denne ekstreme afkøling er opnået, kan hjertelungemaskinen stoppes, og kirurgen kan korrigere meget komplekse aorta- og hjertedefekter under cirkulationsstop. I løbet af denne periode cirkulerer intet blod inde i patienten. Når operationen er afsluttet, opvarmes blodet gradvist i den samme varmeveksler, der bruges til afkøling. Gradvis opvarmning tilbage til normale kropstemperaturer resulterer i genoptagelse af normale hjerne- og organfunktioner. Denne dybe hypotermi er imidlertid langt væk fra frysning og langvarig kryokonservering.
Celler kan leve mere end et årti, hvis de er korrekt frosset. Derudover kan visse væv, såsom parathyreoidea-kirtler, blodårer, hjerteklapper og aortavæv, med held kryoperveres. Frysning bruges også til at opbevare og opretholde langvarig levedygtighed af tidlige menneskelige embryoner, æg (æg) og sædceller. Fryseprocedurerne, der er anvendt til disse væv, er veletablerede, og i nærvær af kryobeskyttelsesmidler kan vævene opbevares over lange perioder ved temperaturer på -14 ° C (6,8 ° F).
Forskning har vist, at hele dyr, som er frosset i fravær af kryobeskyttelsesmidler, kan give levedygtige celler, der indeholder intakt DNA ved optøning. F.eks. Er kerner i hjerneceller fra hele mus, der er opbevaret ved -20 ° C (-4 ° F) i mere end 15 år, blevet brugt til at generere linjer med embryonale stamceller. Disse celler blev derefter anvendt til at fremstille musekloner.