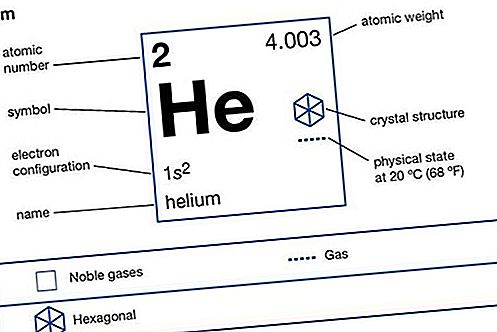
Molybdæn (Mo), kemisk element, sølvgrå ildfast metal fra gruppe 6 (VIb) i det periodiske system, der bruges til at give overlegen styrke til stål og andre legeringer ved høj temperatur.
Den svenske kemiker Carl Wilhelm Scheele havde demonstreret (ca. 1778), at mineralet molybdaina (nu molybdenit), der længe blev antaget at være en blymalm eller grafit, bestemt indeholder svovl og muligvis et tidligere ukendt metal. Efter Schelees forslag isolerede Peter Jacob Hjelm, en anden svensk kemiker, metallet med succes (1782) og kaldte det molybdæn fra det græske molybdos, ”bly”.
Molybdæn findes ikke frit i naturen. Et relativt sjældent element, det er omtrent lige så rigeligt som wolfram, som det ligner. For molybdæn er hovedmalmen molybdenit — molybdendisulfid, MoS 2 - men molybdater såsom blymolybdat, PbMoO 4 (wulfenit) og MgMoO 4 findes også. Mest kommerciel produktion er fra malm, der indeholder mineralet molybdenit. Det koncentrerede mineral ristes normalt i et overskud af luft for at give molybdæntrioxid (MoO 3), også kaldet teknisk molybdisk oxid, som efter oprensning kan reduceres med brint til metallet. Efterfølgende behandling afhænger af den ultimative anvendelse af molybdæn. Molybdæn kan sættes til stål i ovnen i form af enten teknisk oxid eller ferromolybden. Ferromolybden (indeholdende mindst 60 procent molybdæn) produceres ved at antænde en blanding af teknisk oxid og jernoxid. Metallisk molybdæn produceres i form af et pulver ved reduktion med hydrogen af kemisk ren molybdæntrioxid eller ammoniummolybdat, (NH 4) 2 MoO 4. Pulveret omdannes til massivt metal ved pulvermetallurgiprocessen eller ved lysbue-støbningsprocessen.
Molybdæn-base-legeringer og selve metallet har brugbar styrke ved temperaturer over hvilke de fleste andre metaller og legeringer er smeltet. Den største anvendelse af molybdæn er imidlertid som et legeringsmiddel til fremstilling af jernholdige og ikke-jernholdige legeringer, hvortil det unikt bidrager med varm styrke og korrosionsbestandighed, fx i jetmotorer, forbrændingsforinger og efterbrændingsdele. Det er et af de mest effektive elementer til at øge hærdbarheden af jern og stål, og det bidrager også til sejheden af dæmpet og hærdet stål. Den høje korrosionsbestandighed, der kræves i de rustfrie stål, der bruges til behandling af farmaceutiske stoffer og i kromstål til biltrimning, forbedres unikt ved små tilsætninger af molybdæn. Metallisk molybdæn er blevet brugt til sådanne elektriske og elektroniske dele som filamentbærere, anoder og gitter. Stang eller ledning bruges til varmeelementer i elektriske ovne, der arbejder op til 1.700 ° C (3.092 ° F). Overtræk af molybdæn klæber fast til stål, jern, aluminium og andre metaller og viser fremragende modstand mod slid.
Molybdæn er temmelig modstandsdygtig over for angreb fra syrer, undtagen blandinger af koncentreret salpetersyre og fluoridsyrer, og det kan hurtigt angribes af alkalisk oxiderende smelte, såsom smeltede blandinger af kaliumnitrat og natriumhydroxid eller natriumperoxid; vandige alkalier er imidlertid uden virkning. Det er inert over for ilt ved normal temperatur, men kombineres let med det ved rød varme for at give trioxiderne og angribes af fluor ved stuetemperatur for at give hexafluoriderne.
Naturligt molybdæn er en blanding af syv stabile isotoper: molybdæn-92 (15,84 procent), molybdæn-94 (9,04 procent), molybdæn-95 (15,72 procent), molybdæn-96 (16,53 procent), molybdæn-97 (9,46 procent), molybdæn-98 (23,78 procent) og molybdæn-100 (9,13 procent). Molybdæn udviser oxidationstilstande på +2 til +6 og anses for at vise nuloxidationstilstanden i carbonyl Mo (CO) 6. Molybdæn (+6) forekommer i trioxidet, den vigtigste forbindelse, hvorfra de fleste af dets andre forbindelser fremstilles, og i molybdaterne (der indeholder anionen MoO 4 2−), der bruges til at fremstille pigmenter og farvestoffer. Molybdendisulfid (MoS 2), der ligner grafit, bruges som et fast smøremiddel eller som et tilsætningsstof til fedt og olier. Molybdæn danner hårde, ildfaste og kemisk inerte interstitielle forbindelser med bor, carbon, nitrogen og silicium ved direkte reaktion med disse elementer ved høje temperaturer.
Molybdæn er et essentielt sporelement i planter; i bælgplanter som katalysator hjælper det bakterier med at fikse nitrogen. Molybdentrioxid og natriummolybdat (Na 2 MoO 4) er blevet anvendt som mikronæringsstoffer.
De største producenter af molybdæn er Kina, USA, Chile, Peru, Mexico og Canada.
Elementegenskaber
| Atom nummer | 42 |
|---|---|
| atomvægt | 95,94 |
| smeltepunkt | 2.610 ° C (4.730 ° F) |
| kogepunkt | 5.560 ° C (10.040 ° F) |
| specifik tyngdekraft | 10,2 ved 20 ° C (68 ° F) |
| oxidationstilstande | 0, +2, +3, +4, +5, +6 |
| elektronkonfiguration | [Kr] 4d 5 5s 1 |



![Slaget ved Plataea græsk historie [479 fvt] Slaget ved Plataea græsk historie [479 fvt]](https://images.thetopknowledge.com/img/world-history/8/battle-plataea-greek-history-479-bce.jpg)