Ionkanal, protein udtrykt af stort set alle levende celler, der skaber en vej for ladede ioner fra opløste salte, herunder natrium-, kalium-, calcium- og chloridioner, til at passere gennem den ellers uigennemtrængelige lipidcellemembran. Betjening af celler i nervesystemet, sammentrækning af hjertet og knoglemuskler og sekretion i bugspytkirtlen er eksempler på fysiologiske processer, der kræver ionkanaler. Derudover er ionkanaler i membranerne i intracellulære organeller vigtige til regulering af cytoplasmisk calciumkoncentration og forsuring af specifikke subcellulære rum (f.eks. Lysosomer).
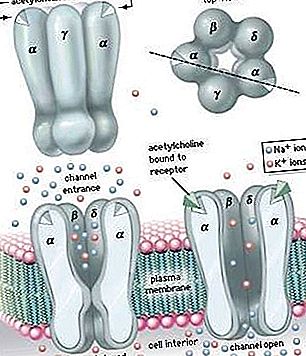
celle: Membrankanaler
Biofysikere, der måler den elektriske strøm, der passerer gennem cellemembraner, har fundet, at cellemembranerne generelt har en langt større
Evolution og selektivitet
Ioner flyder passivt gennem kanaler mod ligevægt. Denne bevægelse kan være drevet af elektriske (spænding) eller kemiske (koncentrations) gradienter. Evnen til at ændre ionstrømmen som et resultat af udviklingen af ionkanaler kan have givet en evolutionær fordel ved at lade encellede organismer regulere deres volumen i lyset af miljøændringer. Gennem efterfølgende udvikling er ionkanaler kommet til at spille vigtige roller i cellulær sekretion og elektrisk signalering.
De fleste ionkanaler er lukket - det vil sige at de åbnes og lukkes enten spontant eller som respons på en bestemt stimulus, såsom binding af et lille molekyle til kanalproteinet (ligand-gatede ionkanaler) eller en ændring i spænding over membranen der registreres af ladede segmenter af kanalproteinet (spændings-gatede ionkanaler). Derudover er de fleste ionkanaler selektive, hvilket kun tillader visse ioner at passere. Nogle kanaler leder kun en type ion (f.eks. Kalium), mens andre kanaler udviser relativ selektivitet - for eksempel tillader positivt ladede kationer at passere, mens de ekskluderede negativt ladede anioner udelukkes. Celler i højere organismer kan udtrykke mere end 100 forskellige typer ionkanal, hver med forskellig selektivitet og forskellige gatingegenskaber.
Funktion og struktur
Strømmen af ladede ioner gennem åbne kanaler repræsenterer en elektrisk strøm, der ændrer spændingen over membranen ved at ændre ladefordelingen. I exciterbare celler undergår spændings-gatede kanaler, der tillader kortvarig tilstrømning af positive ioner (f.eks. Natrium- og calciumioner) kort depolarisering af membranen kendt som handlingspotentialer. Handlingspotentialer kan overføres hurtigt over lange afstande, hvilket muliggør koordinering og præcis timing af fysiologiske output. I næsten alle tilfælde udløser handlingspotentiale nedstrøms fysiologiske virkninger, såsom sekretion eller muskelsammentrækning, ved at åbne spændings-gatede calcium-selektive ionkanaler og hæve den intracellulære calciumkoncentration.
Aminosyresekvenserne af mange forskellige ionkanalproteiner er blevet bestemt, og i nogle få tilfælde er kanalens røntgenkrystallstruktur også kendt. Baseret på deres struktur kan størstedelen af ionkanaler klassificeres i seks eller syv superfamilier. For kaliumselektive kanaler, der er blandt de bedst karakteriserede ionkanaler, mødes fire homologe transmembrane underenheder for at skabe en tunnel, kendt som den ledende pore, der tilvejebringer en polær bane gennem den ikke-polære lipidmembran. Andre kanaltyper kræver enten tre eller fem homologe underenheder for at generere den centrale ledende pore. I opløsning stabiliseres ioner af polariserede vandmolekyler i det omgivende miljø. Smalle, meget selektive ionkanaler efterligner vandmiljøet ved at foret den ledende pore med polariserede carbonyl-oxygenatomer. Mindre-selektive kanaler danner porer med en diameter, der er stor nok til, at ioner og vandmolekyler kan passere sammen.
Toksiner og sygdomme
Mange naturlige toksiner er målrettet mod ionkanaler. Eksempler indbefatter den spænding-gatede natriumkanalblokkerer tetrodotoxin, der produceres af bakterier, der er bosiddende i puffere (blæfisk) og flere andre organismer; den irreversible nikotiniske acetylcholinreceptorantagonist alfa-bungarotoxin fra giftet med slanger i slægten Bungarus (kraits); og planteafledte alkaloider, såsom strychnin og d-tubocurarin, som inhiberer aktiveringen af ionkanaler, der åbnes af henholdsvis neurotransmitterne glycin og acetylcholin. Derudover virker et stort antal terapeutiske medikamenter, herunder lokale anæstetika, benzodiazepiner og sulfonylurinstoffer, direkte eller indirekte til at modulere ionkanalaktivitet.
I arvede mutationer i ionkanalgener og i gener, der koder for proteiner, der regulerer ionkanalaktivitet, er blevet impliceret i en række sygdomme, herunder ataksi (manglende evne til at koordinere frivillige muskelbevægelser), diabetes mellitus, visse typer af epilepsi og hjertearytmier (uregelmæssigheder) i hjerteslag). F.eks. Ligger genetiske variationer i natriumselektive og kaliumselektive kanaler eller i deres tilknyttede regulatoriske underenheder under nogle former for lang-QT-syndrom. Dette syndrom er kendetegnet ved en forlængelse af depolariseringstiden for hjertemyocytvirkningsmuligheder, hvilket kan føre til dødelige arytmier. Derudover ligger mutationer i adenosintrifosfat (ATP) -følsomme kaliumkanaler, der kontrollerer insulinudskillelse fra celler i bugspytkirtlen, nogle former for diabetes mellitus.