Antimon (Sb), et metallisk element, der hører til nitrogengruppen (gruppe 15 [Va] i det periodiske system). Antimon findes i mange allotropiske former (fysisk forskellige betingelser, der er resultatet af forskellige arrangementer af de samme atomer i molekyler eller krystaller). Antimon er et skinnende, sølvfarvet, blåligt hvidt fast stof, der er meget sprødt og har en flassende struktur. Det forekommer hovedsageligt som den grå sulfidmineralstibnit (Sb 2 S 3).
Elementegenskaber
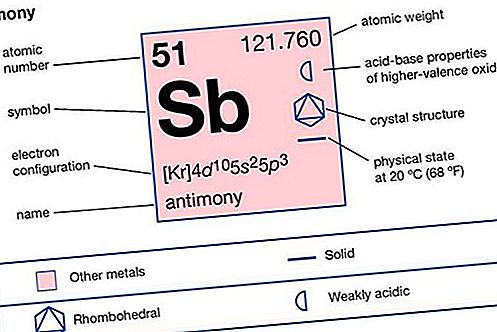
| Atom nummer | 51 |
|---|---|
| atomvægt | 121,75 |
| smeltepunkt | 630,5 ° C (1.166,9 ° F) |
| kogepunkt | 1.380 ° C (2.516 ° F) |
| massefylde | 6,691 g / cm 3 ved 20 ° C (68 ° F) |
| oxidationstilstande | −3, +3, +5 |
| elektronkonfiguration. | 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 5s 2 5p 3 |
Historie
De gamle var bekendt med antimon både som metal og i dets sulfidform. Fragmenter af en kaldeisk vase lavet af antimon er estimeret til dato fra ca. 4000 f.Kr. Det Gamle Testamente fortæller om dronning Jezebel, der bruger det naturligt forekommende sulfid af antimon til at forskønne hendes øjne. Plinius skrev i løbet af det 1. århundrede annoncen om syv forskellige lægemidler, der anvender stibium eller antimonsulfid. Tidlige skrifter af Dioscorides, der stammer fra omkring samme tid, nævner metallisk antimon. Registreringer fra det 15. århundrede viser stoffets anvendelse i legeringer til type, klokker og spejle. I 1615 beskrev Andreas Libavius, en tysk læge, fremstillingen af metallisk antimon ved direkte reduktion af sulfidet med jern; og en senere kemi-lærebog af Lémery, udgivet i 1675, beskriver også metoder til forberedelse af elementet. I det samme århundrede blev en bog, der opsummerer tilgængelig viden om antimon og dens forbindelser, angiveligt skrevet af en Basil Valentine, angiveligt en benediktinermunk fra det 15. århundrede, hvis navn vises på kemiske skrifter i løbet af to århundreder. Navnet antimon synes at være afledt af det latinske antimonium i en oversættelse af et værk af alkymisten Geber, men dets virkelige oprindelse er usikker.
Forekomst og distribution
Antimon er omkring en femtedel så rigelig som arsen, og bidrager i gennemsnit ca. et gram til hvert ton af jordskorpen. Dens kosmiske overflod estimeres til at være omkring et atom til hver 5.000.000 atomer af silicium. Der er fundet små aflejringer af nativt metal, men det meste antimon forekommer i form af mere end 100 forskellige mineraler. Den vigtigste af disse er stibnite, Sb 2 S 3. Små stibnitaflejringer findes i Algeriet, Bolivia, Kina, Mexico, Peru, Sydafrika og i dele af Balkanhalvøen. En vis økonomisk værdi hænger også til kermesite (2Sb 2 S 3 · Sb 2 O 3), argentiferøs tetrahedrit [(Cu, Fe) 12 Sb 4 S 13], livingstonite (HgSb 4 S 7) og jamesonit (Pb 4 FeSb 6 S 14). Små mængder kan også genvindes ved produktion af kobber og bly. Cirka halvdelen af alt det producerede antimon genvindes fra skrot blylegering fra gamle batterier, hvortil antimon blev tilføjet for at give hårdhed.
To stabile isotoper, næsten lige i overflod, forekommer i naturen. Den ene har masse 121 og den anden masse 123. Der er blevet fremstillet radioaktive isotoper af masserne 120, 122, 124, 125, 126, 127, 129 og 132.