Uran (U), radioaktivt kemisk element i actinoid-serien i det periodiske system, atomnummer 92. Det er et vigtigt atombrændstof.
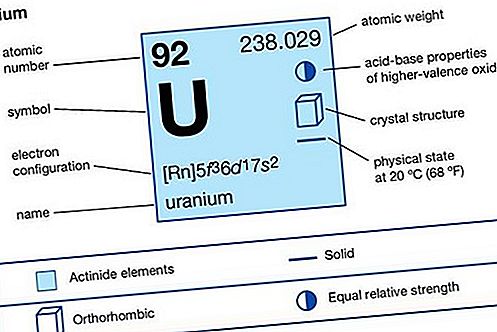

actinoid element
medlemmer af gruppen, inklusive uran (det mest kendte), forekommer naturligt, de fleste er menneskeskabte. Både uran og plutonium er blevet anvendt
Uran udgør omkring to dele pr. Million af jordskorpen. Nogle vigtige uran mineraler er begblende (urent U 3 O 8), uraninit (UO 2), carnotite (kalium uran vanadat), autunit (et calcium- uran phosphat), og torbernite (en kobber uran phosphat). Disse og andre genvindelige uranmalm indeholder som kilder til nukleare brændstoffer mange gange mere energi end alle de kendte genvindelige forekomster af fossile brændstoffer. Et pund uran giver så meget energi som 1,4 millioner kilogram (3 millioner pund) kul.
For yderligere information om uranmalmaflejringer samt dækning af minedrift, raffinering og nyttiggørelsesteknikker, se uranforarbejdning. For sammenlignende statistiske data om uranproduktion, se tabel.
uran
| Land | mineproduktion 2013 (metriske tons) | % af verdens mineproduktion |
|---|---|---|
| *Skøn. | ||
| Kilde: World Nuclear Association, World Uranium Mining Production (2014). | ||
| Kasakhstan | 22.574 | 37,9 |
| Canada | 9332 | 15.6 |
| Australien | 6350 | 10.6 |
| Niger * | 4528 | 7.6 |
| Namibia | 4315 | 7.2 |
| Rusland | 3135 | 5.3 |
| Usbekistan * | 2.400 | 4,0 |
| Forenede Stater | 1.835 | 3.1 |
| Kina* | 1.450 | 2.4 |
| Malawi | 1.132 | 1.9 |
| Ukraine | 1.075 | 1.9 |
| Sydafrika | 540 | 0,9 |
| Indien * | 400 | 0,7 |
| Tjekkiet | 225 | 0,4 |
| Brasilien | 198 | 0,3 |
| Rumænien * | 80 | 0,1 |
| Pakistan * | 41 | 0,1 |
| Tyskland | 27 | 0,0 |
| verdens samlede | 59.637 | 100 |
Uran er et tæt, hårdt metallisk element, der er sølvfarvet i farve. Det er let, formbart og i stand til at tage en høj polering. I luften pletter metallet, og når det er fint opdelt, bryder det i flammer. Det er en relativt dårlig leder af elektricitet. Selvom det blev opdaget (1789) af den tyske kemiker Martin Heinrich Klaproth, der opkaldte det efter den daværende for nylig opdagede planet Uranus, blev selve metallet først isoleret (1841) af den franske kemiker Eugène-Melchior Péligot ved reduktion af urantetrachlorid (UCl 4) med kalium.
Formuleringen af det periodiske system af den russiske kemiker Dmitry Mendeleyev i 1869 fokuserede opmærksomheden på uran som det tyngste kemiske element, en position, som det havde indtil opdagelsen af det første transuraniumelement neptunium i 1940. I 1896 opdagede den franske fysiker Henri Becquerel i uran fænomenet radioaktivitet, et udtryk, der først blev brugt i 1898 af de franske fysikere Marie og Pierre Curie. Denne egenskab blev senere fundet i mange andre elementer. Det vides nu, at uran, radioaktivt i alle dets isotoper, naturligt består af en blanding af uran-238 (99,27 procent, 4.510.000.000-års halveringstid), uran-235 (0,72 procent, 713.000.000-års halveringstid), og uranium-234 (0,006 procent, 247.000 års halveringstid). Disse lange halveringstider muliggør bestemmelse af Jordens alder ved at måle mængden af bly, urans ultimative henfaldsprodukt, i visse uranholdige klipper. Uran-238 er forældrene og uran-234 en af døtrene i den radioaktive uranforfaldsserie; uranium-235 er overordnede til aktiniumfaldsserien. Se også actinoid-element.
Elementet uran blev genstand for intens undersøgelse og bred interesse, efter at de tyske kemikere Otto Hahn og Fritz Strassmann i slutningen af 1938 opdagede fænomenet kerneklydning i uran bombarderet af langsomme neutroner. Den italienske fødte amerikanske fysiker Enrico Fermi foreslog (tidligt i 1939), at neutroner kunne være blandt fissionprodukterne og således kunne fortsætte fission som en kædereaktion. Den ungarske-fødte amerikanske fysiker Leo Szilard, den amerikanske fysiker Herbert L. Anderson, den franske kemiker Frédéric Joliot-Curie, og deres kolleger bekræftede (1939) denne forudsigelse; senere undersøgelser viste, at et gennemsnit på 2 1 / 2 neutroner pr atom frigives under fission. Disse opdagelser førte til den første selvbærende atomkædereaktion (2. december 1942), den første atombomptest (16. juli 1945), den første atombombe faldt i krigsførelse (6. august 1945), den første atomdrevne ubåd (1955) og den første fuldskala-elektriske generator (1957).
Fission sker med langsomme neutroner i den relativt sjældne isotop uran-235 (det eneste naturligt forekommende fissile materiale), som skal adskilles fra det rigelige isotop uran-238 til dets forskellige anvendelser. Uranium-238 overføres imidlertid efter absorption af neutroner og gennemgået negativt beta-henfald til det syntetiske element plutonium, der er spaltet med langsomme neutroner. Naturligt uran kan derfor bruges i konverter- og avlsreaktorer, hvor fission opretholdes af det sjældne uran-235, og plutonium fremstilles på samme tid ved transmutation af uran-238. Fissilt uranium-233 kan syntetiseres til brug som et nukleart brændstof fra den ikke-fissile thorium-isotop Thorium-232, der er rigelig i naturen. Uran er også vigtigt som det primære materiale, hvorfra de syntetiske transuranelementer er blevet fremstillet ved transmutationsreaktioner.
Uran, som er stærkt elektropositivt, reagerer med vand; det opløses i syrer, men ikke i alkalier. De vigtige oxidationstrin er +4 (som i den oxid UO 2, tetrahalides såsom UCL 4, og den grønne vandige ion U 4 +) og +6 (som i oxid UO 3, den hexafluorid UF 6, og den gule uranyl ion UO 2 2+). I en vandig opløsning er uran mest stabilt som uranylionen, der har en lineær struktur [O = U = O] 2+. Uran udviser også en tilstand +3 og +5, men de respektive ioner er ustabile. Den røde U 3+ ion oxideres langsomt, selv i vand, der ikke indeholder opløst ilt. Farven på UO 2 + ion er ukendt, fordi det undergår disproportionering (UO 2 + samtidig reduceres til U 4 + og oxideres til UO 2 2+) selv i meget fortyndede opløsninger.
Uranforbindelser er blevet anvendt som farvestoffer til keramik. Uranhexafluorid (UF 6) er et fast stof med et usædvanligt højt damptryk (115 torr = 0,15 atm = 15,300 Pa) ved 25 ° C (77 ° F). UF 6 er kemisk meget reaktiv, men på trods af sin ætsende karakter i damptilstand er UF 6 blevet vidt brugt i gasdiffusions- og gassentrifuge-metoder til adskillelse af uranium-235 fra uranium-238.
Organometalliske forbindelser er en interessant og vigtig gruppe af forbindelser, hvor der er metal-carbonbindinger, der binder et metal til organiske grupper. Uranocene er en organouranium forbindelse U (C 8 H 8) 2, i hvilken en uran atom er indlagt mellem to organiske ring lag relateret til cyclooctatetraen C 8 H 8. Opdagelsen i 1968 åbnede et nyt område inden for organometallisk kemi.
Elementegenskaber
| Atom nummer | 92 |
|---|---|
| atomvægt | 238,03 |
| smeltepunkt | 1.132,3 ° C (2.070.1 ° F) |
| kogepunkt | 3.818 ° C (6.904 ° F) |
| specifik tyngdekraft | 19.05 |
| oxidationstilstande | +3, +4, +5, +6 |
| elektronkonfiguration af gasformig atomtilstand | [Rn] 5f 3 6d 1 7s 2 |













